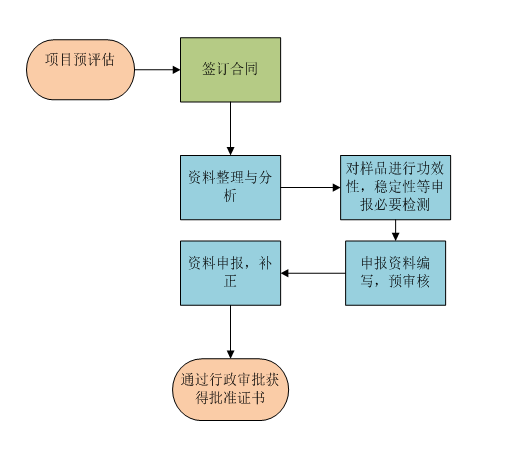
对产品相关资料进行收集与分析,包括技术资料、证明文件、科学文献等。对样品进行安全性、保健功能、功效成分、卫生学、稳定性等申报必要检验。对申报资料进行编制,跟进申报流程,协助提交补正资料,现场核查等
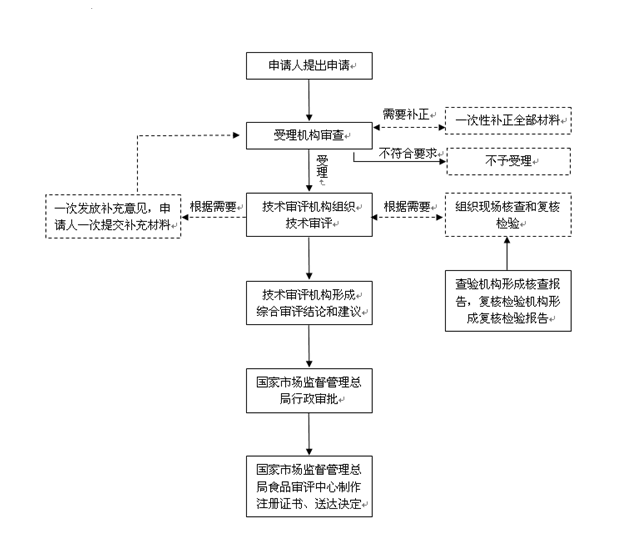
国产保健食品申请者应提交的材料有:
1.保健食品注册申请表
2.申请人营业执照或身份证或其它机构合法登记证明文件复印件
3.保健食品的通用名称与已经批准注册的药品名称不重名的检索材料
4.申请人对他人已取得的专利不构成侵权的保证书
5.商标注册证复印件(未注册商标的不需提供)
6.产品研发报告
7.产品配方及配方依据,原辅料的来源及使用依据
8.功效成分/标志性成分、含量及功效成分/标志性成分的检验方法
9.生产工艺简图、详细说明及有关的研究资料
10.产品质量标准(企业标准)和起草说明以及原辅料的质量标准
11.直接接触产品的包装材料的种类、名称、质量标准及选择依据
12.检验机构出具的检验报告
13.产品标签、说明书样稿
14.其它有助于产品审评的资料
15.未启封的最小销售包装的样品2件
进口保健食品申请者应提交的材料有:
1.进口保健食品注册申请表
2.商标注册证复印件
3.保健食品的中文名称与已经批准注册的药品名称不重名的检索材料
4.申请人对他人已取得专利不构成侵权的保证书
5.商标注册证复印件
6.产品研发报告
7.产品配方(原.辅料原文以及中文译本)及配方依据,原.辅料的来源及使用依据和质量标准
8.功效成份.含量及功效成份的检验方法
9.生产工艺详细说明.简图(原文及中文译本)和有关的研究资料
10.产品质量标准(企业标准原本及中文译本)和起草说明以及原辅料的质量标准
11.直接接触产品的材料和质量标准及选择依据
12.检验机构出具的检验报告
13产品标签.产品说明书样稿
14.生产国或地区有关机构出具的该生产企业符合当地相应生产质量管理规范的证明文件.
15.委托申报提供经公证的委托书原件及受委托的代理机构的营业执照复印件境外厂商常驻中国代表机构办理注册事务的,提供<外国企业长驻中国代表机构登记证>复印件
16.产品在生产国(地区)生产销售1年以上的证明文件
17.生产国(地区)或国际组织与产品相关的有关标准
18.产品在生产国(地区)上市使用的包装.标签.说明书实样,并附中文译本
19.其他有助于产品审评的资料
20.未启封的最小销售包装的样品2件.
咨询电话:020-32643645 18028674076
微信:18028674076
地址1:广州市生物岛寰宇三路36号官洲生命科学创新中心B栋411-412单元
地址2:广州市黄埔区科学城揽月路3号广州国际企业孵化器F区F911室-F919室

邮箱:scprs@sccip.org.cn
电话:020-32643642 18027296587
地址:广州市黄埔区科学城揽月路3号广州国际企业孵化器F区720室、广州市黄埔区科学城揽月路3号广州国际企业孵化器F区911室-F919室