生物等效性试验是指仿制药品以上市注册为目的,为确定药物安全性与有效性在人体开展的药物研究。
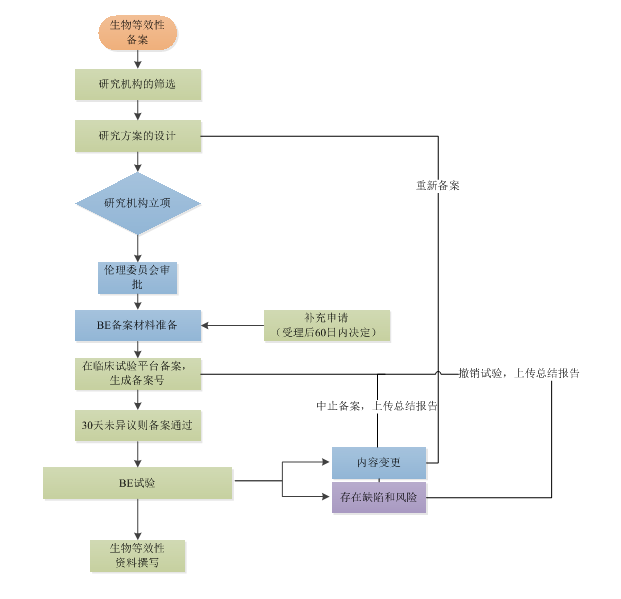
注册申请人可向国家药品监督管理局药品审评中心提交生物等效性备案,备案通过后,申请人可开展生物等效性试验。
|
阶段 |
服务内容 |
时间预估 |
|
咨询阶段 |
提供法规咨询,项目调研,提供服务方案及报价。 |
|
|
立项阶段 |
与客户达成合作,签订各项合同,成立项目组,制定具体项目实施方案及计划,项目组启动立项。 |
|
|
申请资料准备 |
根据客户需求,协助整理各阶段实验数据,撰写综述类与总结类申报资料。 提供模板,按照SOP协助客户完成申请资料准备。 组织专家对撰写的资料进行预审和可行性评估,根据评估情况,进一步完善申报资料。 |
|
|
递交申请 |
帮助客户完成递交申请,实时跟进进度并定期汇报。 |
|
|
临床试验相关服务 |
提供药物临床试验机构调研服务,帮助客户联系CRO公司。 协助客户对研发过程中的问题与CDE进行沟通交流。 |
|
在化学药品领域,我司可提供注册咨询服务;行业年度分析报告调研服务;化学药品相关法规、标准培训;文献、专利等信息检索;协助现场核查及问题整改;预审与撰写注册申报资料等服务,如有需要,可咨询华南新药注册申报服务有限公司。
咨询电话:020-32643645 18027296587
地址1:广州市黄埔区科学城揽月路3号广州国际企业孵化器F区F720室
地址2:广州市黄埔区科学城揽月路3号广州国际企业孵化器F区F911室-F919室

邮箱:scprs@sccip.org.cn
电话:020-32643642 18027296587
地址:广州市黄埔区科学城揽月路3号广州国际企业孵化器F区720室、广州市黄埔区科学城揽月路3号广州国际企业孵化器F区911室-F919室